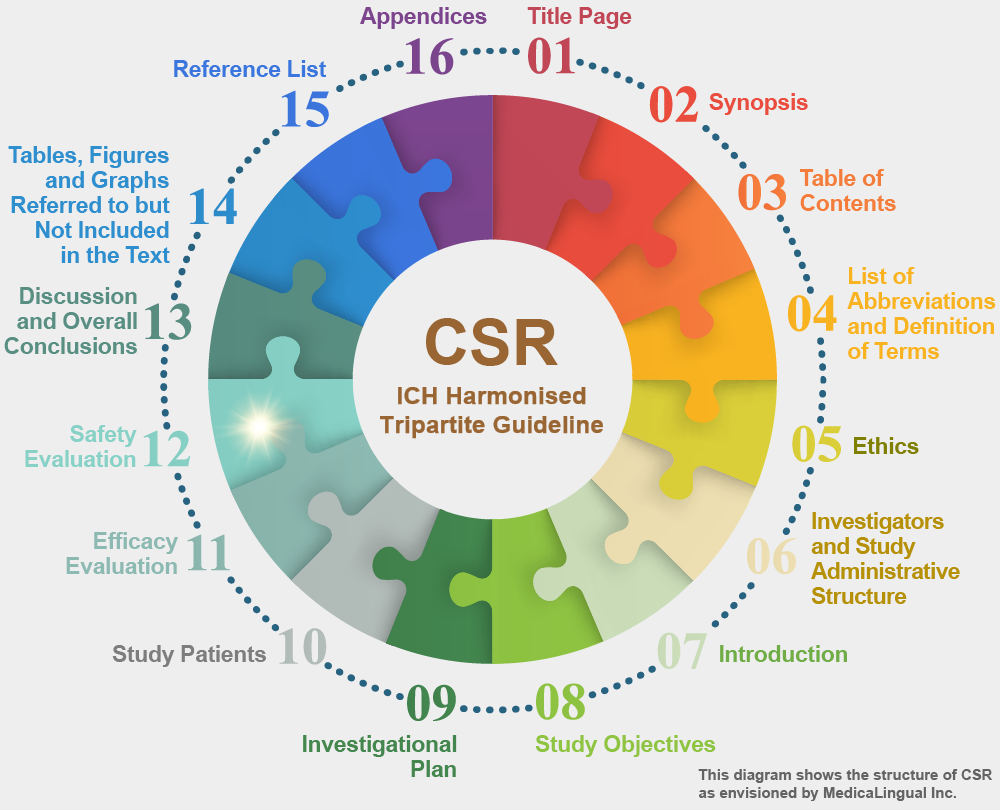
治験の統括報告書の構成と内容に関するガイドライン
平成8年5月1日 薬審第335号
各都道府県衛生主管部(局)長あて 厚生省薬務局審査課長通知
STRUCTURE AND CONTENT OF CLINICAL STUDY REPORTS
Recommended for Adoption at Step 4 of the ICH Process on 30 November 1995 by the ICH Steering Committee
12. 安全性の評価
12.3 死亡,その他の重篤な有害事象及び他の重要な有害事象
12.3.3 死亡,その他の重篤な有害事象及び他の重要な有害事象の分析及び考察
死亡,その他の重篤な有害事象及び投与中止,用量減量,又は併用療法の開始を招いた他の重要な有害事象の重要性を治験薬の安全性の観点から評価すること。これらの事象のいずれについても,当該治験薬に関しては以前には疑われていなかった重要な副作用であるか否かについて特に注意を払わなければならない。特に重要と思われる重篤な有害事象については,生命表又は類似の分析を用い,治験薬の投与時間との関係を示し,経時的に危険性を評価することが役立つこともある。
12. SAFETY EVALUATION
12.3 DEATHS, OTHER SERIOUS ADVERSE EVENTS, AND OTHER SIGNIFICANT ADVERSE EVENTS
12.3.3 ANALYSIS AND DISCUSSION OF DEATHS, OTHER SERIOUS ADVERSE EVENTS AND OTHER SIGNIFICANT ADVERSE EVENTS
The significance of the deaths, other serious adverse events and other significant adverse events leading to withdrawal, dose reduction or institution of concomitant therapy should be assessed with respect to the safety of the test drug/investigational product. Particular attention should be paid to whether any of these events may represent a previously unsuspected important adverse effect of the test drug/investigational product. For serious adverse events that appear of particular importance, it may be useful to use life table or similar analyses to show their relation to time on test drug/investigational product and to assess their risk over time.










