薬生薬審発0202第1号(平成29年2月2日)
ICH HARMONISED GUIDELINE- M4E(R2) – Dated 15 June 2016
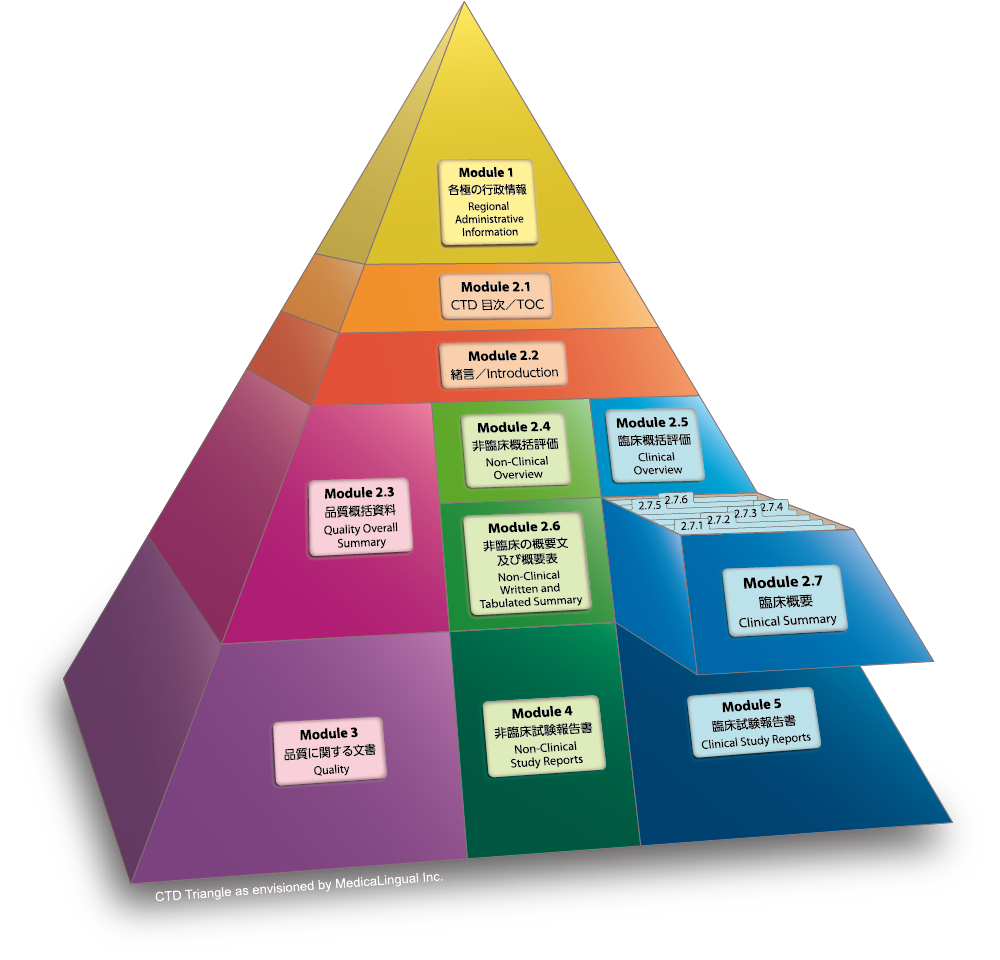
Module 2.7 臨床概要
2.7.4 臨床的安全性の概要
本項では、個々の総括報告書及び他の関連する報告書(例:一部地域にて通常提出されている安全性に関する統合解析)の結果をまとめ、対象となる患者集団における申請医薬品の安全性に関するデータを要約すること。安全性関連データの示し方は、次の三つのレベルで考察することができる(ICH E3)。
- 曝露状況(投与量、投与期間、患者数、患者のタイプ)を検討し、データベースからどの程度の安全性評価が可能なのかを決定すること。
- 比較的よくみられる有害事象や臨床検査値の変化を明確にし、妥当な方法で分類し、それらの発現に関する要約を行うこと。
- 重篤な有害事象(ICH E2Aによる定義)及びその他の重要な有害事象(ICH E3による定義)を明確にし、それらの発現について要約すること。これら事象の頻度を、特に長期にわたり使用される可能性がある医薬品については、経時的に検討すること。
全ての臨床的安全性データを解析し、得られた申請医薬品の安全性プロフィールは、図表を使って詳細に、明確に、客観的に概説すること。
Module 2.7 CLINICAL SUMMARY
2.7.4 Summary of Clinical Safety
This section should be a summary of data relevant to safety in the intended patient population, integrating the results of individual clinical study reports as well as other relevant reports, e.g., the integrated analyses of safety that are routinely submitted in some regions.
The display of safety-related data can be considered at three levels (ICH E3):
- The extent of exposure (dose, duration, number of patients, type of patients) should be examined to determine the degree to which safety can be assessed from the database.
- The more common adverse events and changes in laboratory tests should be identified and classified, and their occurrence should be summarised.
- Serious adverse events (defined in ICH E2A) and other significant adverse events (defined in ICH E3) should be identified and their occurrence should be summarised. These events should be examined for frequency over time, particularly for drugs that may be used chronically.
The safety profile of the drug, described on the basis of analysis of all clinical safety data, should be outlined in a detailed, clear, and objective manner, with use of tables and figures.










