薬生薬審発0202第1号(平成29年2月2日)
ICH HARMONISED GUIDELINE- M4E(R2) – Dated 15 June 2016
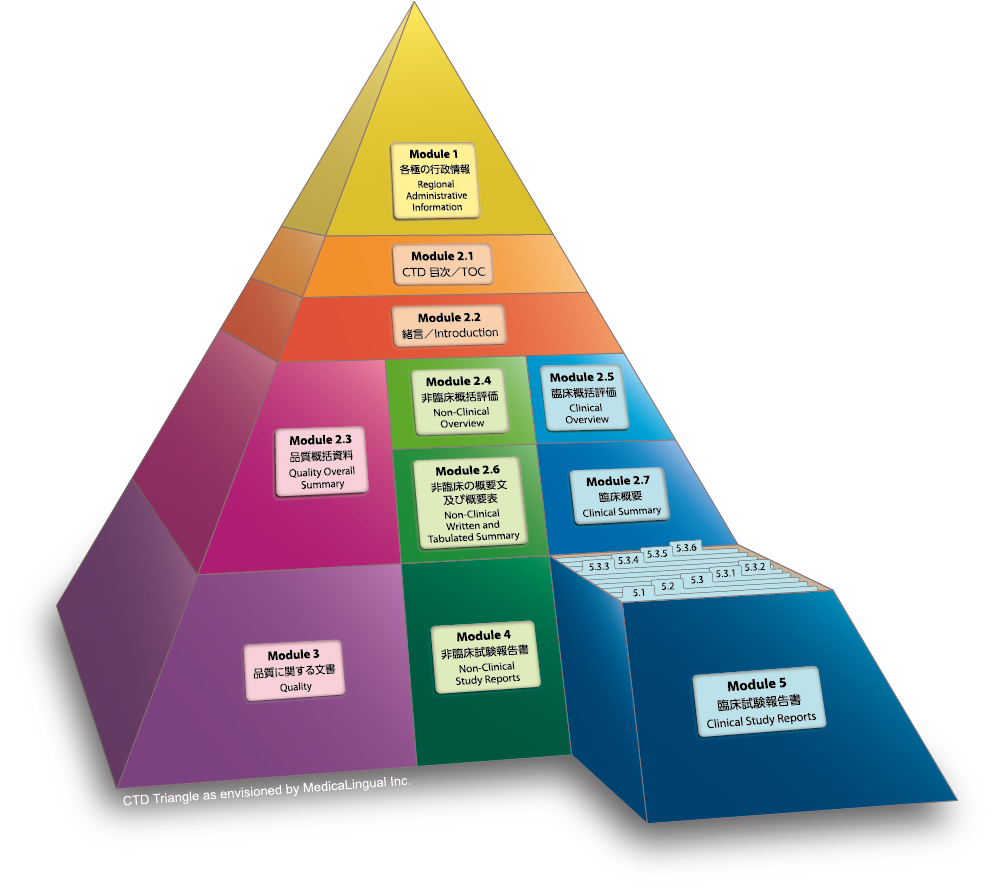
Module 5 臨床試験報告書
5.3 試験報告書及び関連情報
5.3.6 市販後の使用経験に関する報告書
現在市販されている製品については、市販後の使用経験(全ての重要な安全性に関する知見を含む)をまとめた報告書を第5.3.6項に添付すること。
Module 5 CLINICAL STUDY REPORTS
5.3 Clinical Study Reports
5.3.6 Reports of Post-Marketing Experience
For products that are currently marketed, reports that summarize marketing experience (including all significant safety observations) should be included in Section 5.3.6.










