医薬審発第899号 CTD通知(別紙 4)
CTD 非臨床に関する文書の作成要領に関するガイドライン
(2002年9月11-12日ワシントン会議修正版)
ICH HARMONISED GUIDELINE – M4S –
(Numbering and Section Headers have been edited for consistency and use in e-CTD as agreed at the Washington DC Meeting, September 11-12, 2002)
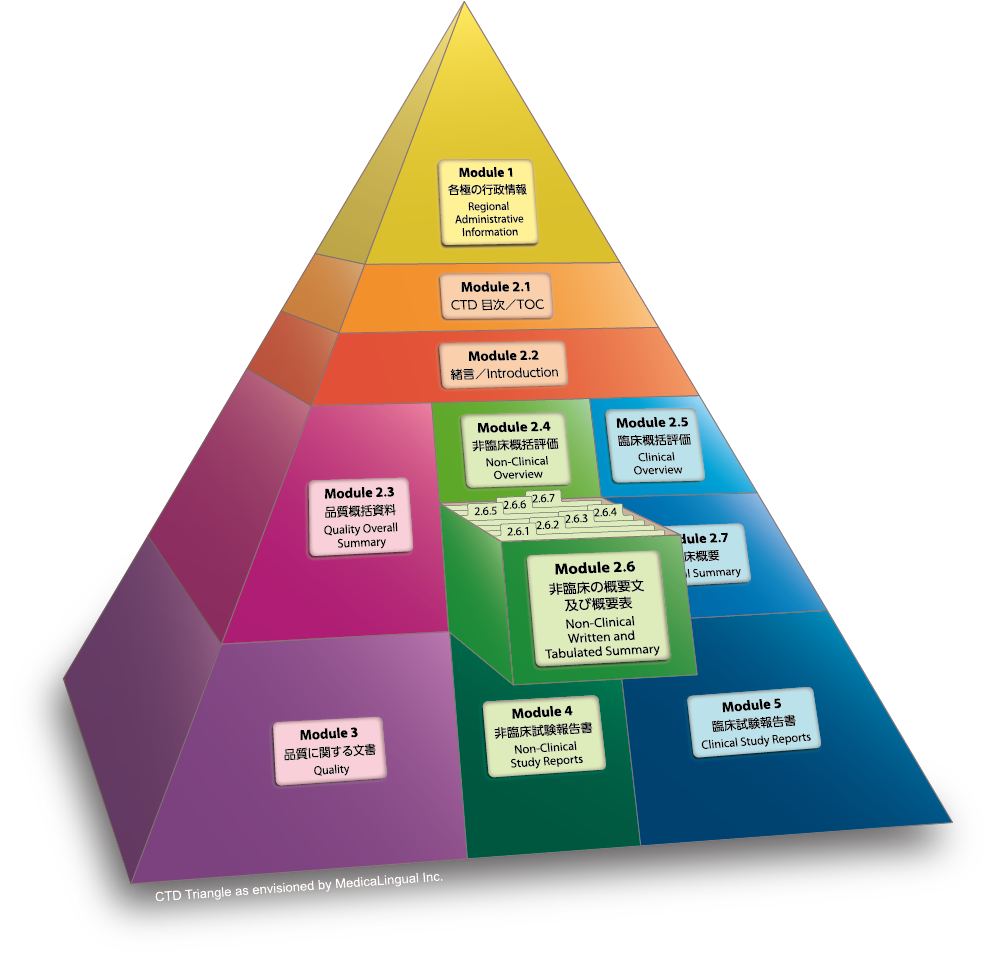
Module 2.6 非臨床試験の概要文及び概要表
2.6.1 緒言
本項の目的は、審査官に医薬品及びその臨床適応を説明することであり、以下の要素を含むこと。
- 医薬品の構造(できるだけ構造式を示すこと)及び薬理的特性に関する簡潔な情報
- 申請された臨床適応、用量及び投与期間に関する情報
Module 2.6 NONCLINICAL WRITTEN AND TABULATED SUMMARIES
2.6.1 Introduction
The aim of this section should be to introduce the reviewer to the pharmaceutical and to its proposed clinical use. The following key elements should be covered:
- Brief information concerning the pharmaceutical’s structure (preferably, a structure diagram should be provided) and pharmacologic properties.
- Information concerning the pharmaceutical’s proposed clinical indication, dose, and duration of use.










