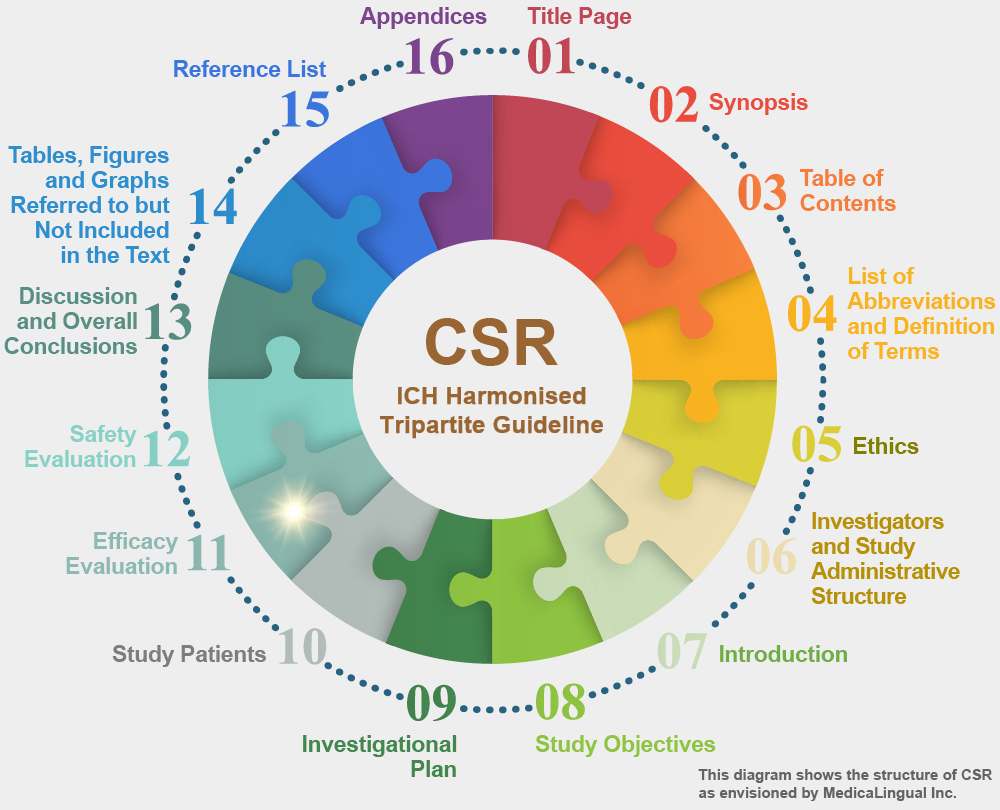
治験の統括報告書の構成と内容に関するガイドライン
平成8年5月1日 薬審第335号
各都道府県衛生主管部(局)長あて 厚生省薬務局審査課長通知
STRUCTURE AND CONTENT OF CLINICAL STUDY REPORTS
Recommended for Adoption at Step 4 of the ICH Process on 30 November 1995 by the ICH Steering Committee
11. 有効性の評価
11.1 解析したデータセット
有効性の各解析に採用した患者を正確に定義すること。例えば,治験薬を投与された全ての患者,有効性に関する何らかの観察が行われたか又は一定の最小限の数の観察が行われた全ての患者,治験を完了した患者のみ,特定の時間範囲内に観察が行われた全ての患者,規定された程度に服薬遵守した患者のみなど。治験実施計画書に定義がない場合は,解析したデータの採用・除外基準が,いつ(開鍵との関連において),どのようにして設けられたのかを明らかにすること。申請者の提案した主たる解析が,たとえデータのそろった患者に限定した部分集団に基づいたものであったとしても,有効性の検証を意図した治験においては,原則として無作為化した(又は組み入れた)全患者の中で何らかの治療中のデータのある全ての患者を対象とした解析を行い,それを追加すること。
11. EFFICACY EVALUATION
11.1 DATA SETS ANALYSED
Exactly which patients were included in each efficacy analysis should be precisely defined, e.g., all patients receiving any test drugs/investigational products, all patients with any efficacy observation or with a certain minimum number of observations, only patients completing the trial, all patients with an observation during a particular time window, only patients with a specified degree of compliance etc. It should be clear, if not defined in the study protocol, when, (relative to study unblinding), and how inclusion/exclusion criteria for the data sets analysed were developed. Generally, even if the applicant’s proposed primary analysis is based on a reduced subset of the patients with data, there should also be for any trial intended to establish efficacy an additional analysis using all randomised (or otherwise entered) patients with any on-treatment data.
有効性の解析から除外した全ての患者,来院時点及び観察データを付録16.2.3の中で一覧表にすること(例として,本ガイドライン別添Ⅵを参照)。また,全ての治療群の全期間にわたって,除外理由も分析すること(例として,本ガイドライン別添Ⅶを参照)。
There should be a tabular listing of all patients, visits and observations excluded from the efficacy analysis provided in appendix 16.2.3 (see Annex VI of the guideline for an example). The reasons for exclusions should also be analysed for the whole treatment group over time (see Annex VII of the guideline for an example).
ガイドライン ― Q&A
解析したデータセット
Q11:「11.1解析したデータセット」の記述について留意すべきことを伺いたい。
A11:すべての解析において,その解析がどのデータセットを対象としてなされたかを報告書に明示することが重要である。また,データの一部を解析から除外した場合には,そのようなデータの選別がいつどのような手順で行われたかを説明する必要がある。
また,有効性の検証を意図した治験の検証対象となる事項の解析において,データの一部を解析から除外した場合には,例えば,服薬したすべての対象における解析や,使用可能なすべてのデータを用いた解析を追加して記載することが求められている。
***










