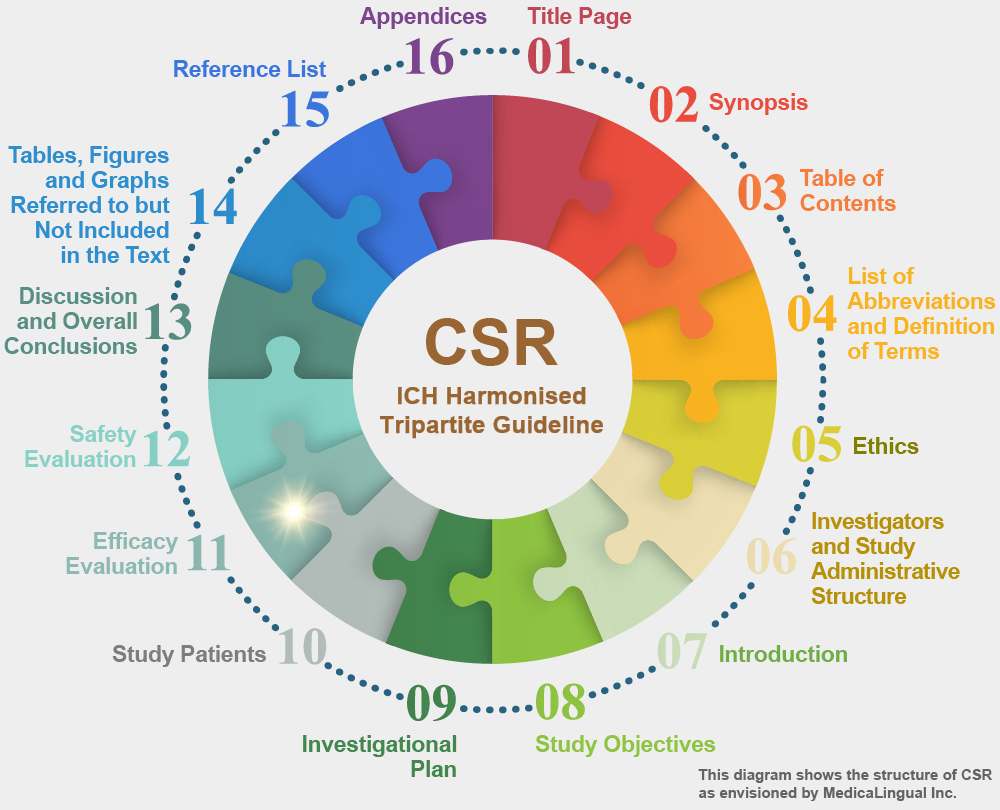
治験の統括報告書の構成と内容に関するガイドライン
平成8年5月1日 薬審第335号
各都道府県衛生主管部(局)長あて 厚生省薬務局審査課長通知
STRUCTURE AND CONTENT OF CLINICAL STUDY REPORTS
Recommended for Adoption at Step 4 of the ICH Process on 30 November 1995 by the ICH Steering Committee
11. 有効性の評価
11.4 有効性に関する成績及び個別患者データ一覧表
11.4.4 薬剤の用量,薬物濃度及びそれらと反応との関係
各患者により用量が異なる場合は,患者ごとの実際に投与された用量を示し,個々の患者の用量を一覧表にすること。用量-反応試験としてデザインされていない試験では,得られる用量-反応情報に限度があるかもしれないが,入手可能なデータからどのような情報が得られるかについて検討すること。用量-反応関係を検討する際,体重あたりの用量(mg/kg)又は体表面積あたりの用量(mg/m2)を計算することが役立つこともある。
11. EFFICACY EVALUATION
11.4 EFFICACY RESULTS AND TABULATIONS OF INDIVIDUAL PATIENT DATA
11.4.4 DRUG DOSE, DRUG CONCENTRATION, AND RELATIONSHIPS TO RESPONSE
When the dose in each patient can vary, the actual doses received by patients should be shown and individual patient’s doses should be tabulated. Although studies not designed as dose-response studies may have limited ability to contribute dose-response information, the available data should be examined for whatever information they can yield. In examining the dose response, it may be helpful to calculate dose as mg/kg body weight or mg/m² body surface.
薬物濃度情報が利用できるならば,それらを一覧表にし(付録16.2.5),可能であれば薬物動態学的観点から分析し,反応と関連づけること。用量-反応又は濃度-反応を探索する試験のデザイン及び分析の手引きとして,ICH ガイドライン「新医薬品の承認に必要な用量-反応関係の検討のための指針」も参照することができる。
Drug concentration information, if available, should also be tabulated (Appendix 16.2.5), analysed in pharmacokinetic terms and, if possible, related to response. Further guidance on the design and analysis of studies exploring dose-response or concentration response can be found in the ICH Guideline “Dose-Response Information to Support Drug Registration”.










