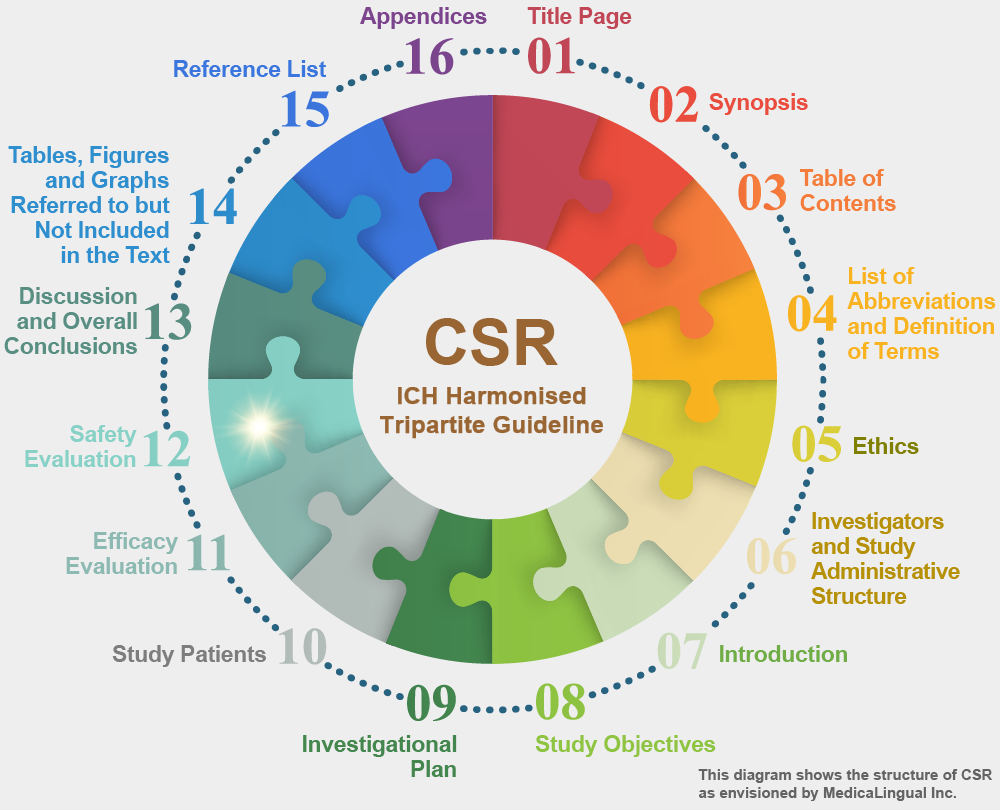
治験の統括報告書の構成と内容に関するガイドライン
平成8年5月1日 薬審第335号
各都道府県衛生主管部(局)長あて 厚生省薬務局審査課長通知
STRUCTURE AND CONTENT OF CLINICAL STUDY REPORTS
Recommended for Adoption at Step 4 of the ICH Process on 30 November 1995 by the ICH Steering Committee
12. 安全性の評価
12.2 有害事象
12.2.1 有害事象の簡潔な要約
治験中に発現した全ての有害事象の経験を叙述形式で簡潔に述べ,後述のより詳細な一覧表及び分析によって補足すること。これらの一覧表及び分析において,被験薬と対照治療のいずれに関連している事象も表示すること。
12. SAFETY EVALUATION
12.2 ADVERSE EVENTS (AEs)
12.2.1 BRIEF SUMMARY OF ADVERSE EVENTS
The overall adverse event experience in the study should be described in a brief narrative, supported by the following more detailed tabulations and analyses. In these tabulations and analyses, events associated with both the test drug and control treatment should be displayed.










