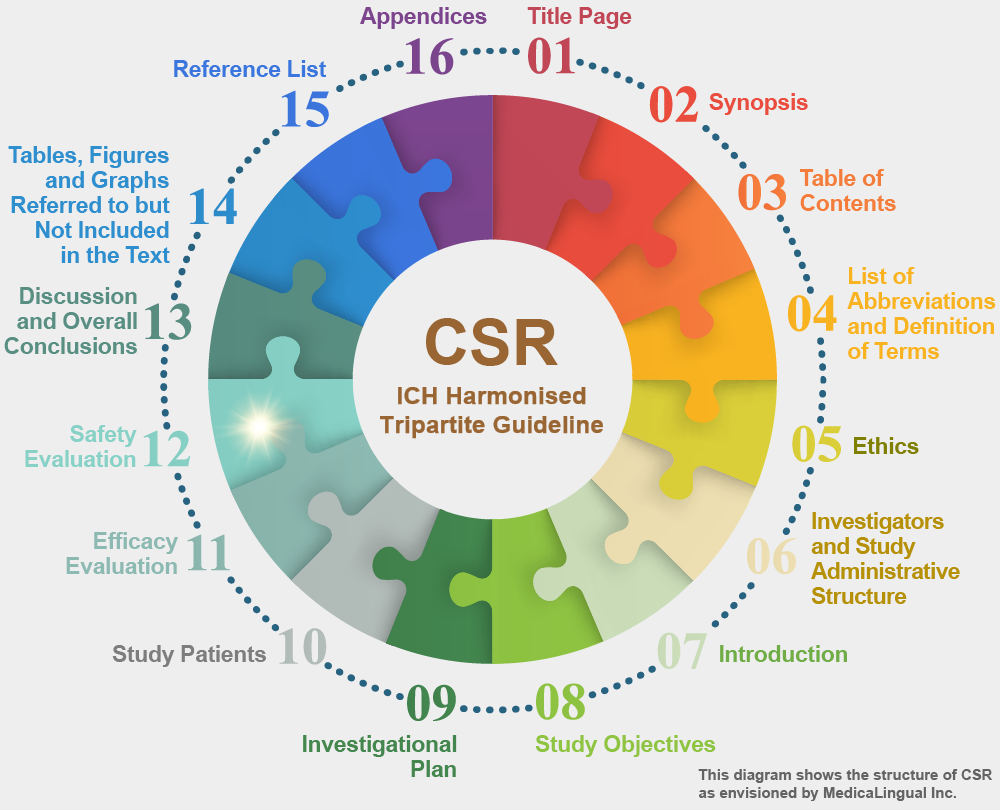
治験の統括報告書の構成と内容に関するガイドライン
平成8年5月1日 薬審第335号
各都道府県衛生主管部(局)長あて 厚生省薬務局審査課長通知
STRUCTURE AND CONTENT OF CLINICAL STUDY REPORTS
Recommended for Adoption at Step 4 of the ICH Process on 30 November 1995 by the ICH Steering Committee
12. 安全性の評価
12.3 死亡,その他の重篤な有害事象及び他の重要な有害事象
12.3.1 死亡,その他の重篤な有害事象及び他の重要な有害事象の一覧表
以下の事象について,上述の12.2.4項で要求された情報と同じものを含む一覧表を作成すること。
12. SAFETY EVALUATION
12.3 DEATHS, OTHER SERIOUS ADVERSE EVENTS, AND OTHER SIGNIFICANT ADVERSE EVENTS
12.3.1 LISTING OF DEATHS, OTHER SERIOUS ADVERSE EVENTS AND OTHER SIGNIFICANT ADVERSE EVENTS
Listings, containing the same information as called for in section 12.2.4 above, should be provided for the following events.
12.3.1.1 死亡
治療後の追跡期間も含め治験中に発生した死亡,及び治験中に始まった変化の結果として生じた死亡の全てについて,14.3.2項で患者ごとに一覧表示すること。
12.3.1.1 Deaths
All deaths during the study, including the post treatment follow-up period, and deaths that resulted from a process that began during the study, should be listed by patient in section 14.3.2.
12.3.1.2 その他の重篤な有害事象
全ての重篤な有害事象(死亡ではないが,時間的に死亡に関連する又は死亡に先行する重篤な有害事象を含む)を14.3.2項で一覧表示すること。この一覧表には,重篤な有害事象と思われた臨床検査値異常,異常なバイタルサイン及び異常な身体的観察項目を含めること。
12.3.1.2 Other Serious Adverse Events
All serious adverse events (other than death but including the serious adverse events temporally associated with or preceding the deaths) should be listed in section 14.3.2. The listing should include laboratory abnormalities, abnormal vital signs and abnormal physical observations that were considered serious adverse events.
12.3.1.3 他の重要な有害事象
重篤な有害事象として報告されているもの以外で,著しい血液学的異常や他の臨床検査値異常(重篤という定義を満たすもの以外)及びそれにより治験薬治療の中止,減量,又は重要な併用療法の追加を含む処置をせざるを得なかった全ての事象を14.3.2項で一覧表示すること。
12.3.1.3 Other Significant Adverse Events
Marked haematological and other laboratory abnormalities (other than those meeting the definition of serious) and any events that led to an intervention, including withdrawal of test drug/investigational product treatment, dose reduction, or significant additional concomitant therapy, other than those reported as serious adverse events, should be listed in section 14.3.2.










