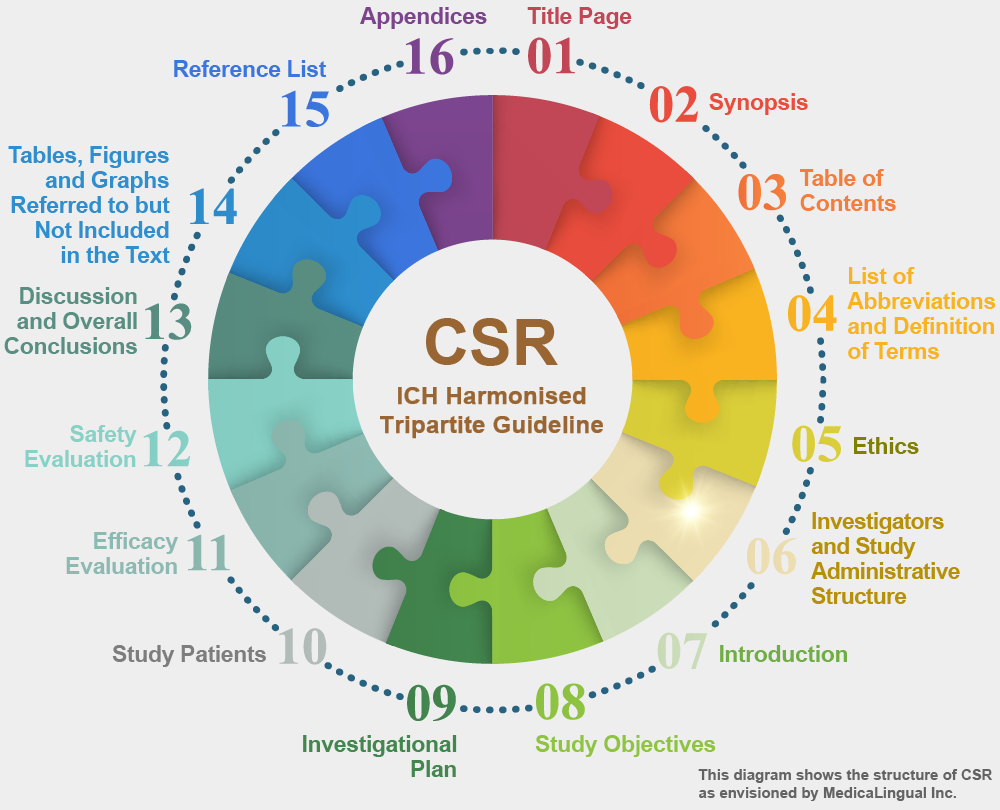
治験の統括報告書の構成と内容に関するガイドライン
平成8年5月1日 薬審第335号
各都道府県衛生主管部(局)長あて 厚生省薬務局審査課長通知
STRUCTURE AND CONTENT OF CLINICAL STUDY REPORTS
Recommended for Adoption at Step 4 of the ICH Process on 30 November 1995 by the ICH Steering Committee
6. 治験責任医師等及び治験管理組織
治験の管理組織(例えば,治験総括(調整)医師,運営委員会,管理・モニタリング・評価委員会,研究機関,統計担当者,臨床検査等の中央測定施設,開発業務受託機関(CRO),治験資材の管理)を簡潔に本文中で説明すること。
6. INVESTIGATORS AND STUDY ADMINISTRATIVE STRUCTURE
The administrative structure of the study (e.g., principal investigator, coordinating investigator, steering committee, administration, monitoring and evaluation committees, institutions, statistician, central laboratory facilities, contract research organisation (C.R.O.), clinical trial supply management) should be described briefly in the body of the report.
治験責任医師等の氏名,所属,治験における役割及び資格(履歴書又はそれに準じるもの)の一覧表を付録16.1.4に添付すること。治験実施に実質的な影響を及ぼした他の参加者についての同様の一覧表もまた16.1.4に添付すること。多数の治験責任医師が参加する大規模試験の場合には,治験における役割によっては,この一覧表は以下のように省略してもよい。すなわち,各治験責任医師や他の参加者の氏名,学位及び研究機関内での所属のみからなる一般的な資格並びに治験における役割の記述にとどめてもよい。
There should be provided in appendix 16.1.4 a list of the investigators with their affiliations, their role in the study and their qualifications (curriculum vitae or equivalent). A similar list for other persons whose participation materially affected the conduct of the study should also be provided in appendix 16.1.4. In the case of large trials with many investigators the above requirements may be abbreviated to consist of general statements of qualifications for persons carrying out particular roles in the study with only the name, degree and institutional affiliation and roles of each investigator or other participant.
一覧表には下記の記述を含めること。
a)治験責任医師
b)看護婦,医師補助員,臨床心理学者,臨床薬剤師,病院勤務医などのうち,効果に関する主要な又は重要な変数の観察を行った全ての人々。ただし,副作用に対する処置をした当直医や,上記のいずれかの人の臨時の代理など,一時的な役割を果たしただけの人については,この一覧表に記載する必要はない。
c)報告書の著者(生物統計担当責任者を含む)
The listing should include:
a) Investigators
b) Any other person carrying out observations of primary or other major efficacy variables, such as a nurse, physician’s assistant, clinical psychologist, clinical pharmacist, or house staff physician. It is not necessary to include in this list a person with only an occasional role, e.g., an on-call physician who dealt with a possible adverse effect or a temporary substitute for any of the above
c) The author(s) of the report, including the responsible biostatistician(s).
治験総括(調整)医師又は治験依頼者の医学責任者の署名を付録16.1.5(書式見本は別添Ⅱを参照)に添付すること。
Where signatures of the principal or coordinating investigators are required by regulatory authorities, these should be included in appendix 16.1.5 (see Annex II for a sample form).
Where these are not required, the signature of the sponsor’s responsible medical officer should be provided in appendix 16.1.5.
ガイドラインQ&A
治験実施組織および構成メンバー
Q6:治験を実施する組織及びその構成メンバーの役割は何か。
A6:治験を実施する国により,あるいは治験の目的や性格付けによって,多様な組織及び役割分担で治験を実施することが可能と考えられ,また,できる限り適切な治験組織及び役割分担を工夫して実施すべきである。それゆえ,治験総括報告書では誰が治験組織に参加し,どのような役割や機能を分担したのかを具体的に記すこととされている。
例えば,安全性委員会やデータモニタリング委員会を設置したのであれば,それらの委員会を構成する委員及び委員会の役割,機能を報告書に記載していただきたい。
Q7:データモニタリング委員会とは何か。
A7:データモニタリング委員会とは,治験の進行や,安全性情報,有効性に関する主要エンドポイントについて,治験途中で予め定めた手順に従って評価し,治験依頼者に治験の継続,変更,中止等を提言することを目的として設置される委員会である。名称は必ずしもこの名前である必要はなく,例えば抗悪性腫瘍薬ガイドラインにある「効果・安全性評価委員会」がこの機能を果たすことも考えられる。
***










