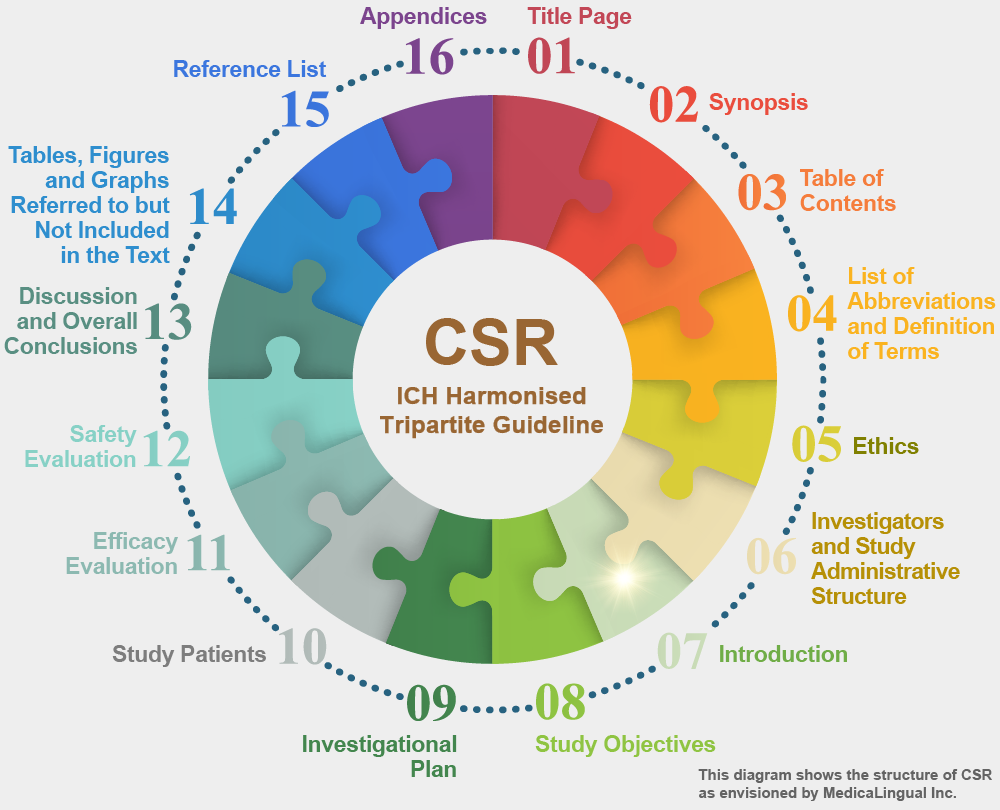
治験の統括報告書の構成と内容に関するガイドライン
平成8年5月1日 薬審第335号
各都道府県衛生主管部(局)長あて 厚生省薬務局審査課長通知
STRUCTURE AND CONTENT OF CLINICAL STUDY REPORTS
Recommended for Adoption at Step 4 of the ICH Process on 30 November 1995 by the ICH Steering Committee
7. 緒言
緒言には,被験薬の開発における当該治験の位置づけ及びその開発に関連する当該治験の特に重要な特徴(例えば,実施の根拠と目的,対象母集団,治療法,期間,主要評価項目)についての簡潔な記述(最高1ページ)を含めること。治験実施計画書の作成の基となったガイドライン,又は当該治験に関して治験依頼者と審査当局との間に交わされた合意事項・会合について,明示又は記述すること。
7. INTRODUCTION
The introduction should contain a brief statement (maximum: 1 page) placing the study in the context of the development of the test drug/investigational product, relating the critical features of the study (e.g., rationale and aims, target population, treatment, duration, primary endpoints) to that development. Any guidelines that were followed in the development of the protocol or any other agreements/meetings between the sponsor/company and regulatory authorities that are relevant to the particular study, should be identified or described.










