医薬審発第899号 CTD通知(別紙 4)
CTD 非臨床に関する文書の作成要領に関するガイドライン
(2002年9月11-12日ワシントン会議修正版)
ICH HARMONISED GUIDELINE – M4S –
(Numbering and Section Headers have been edited for consistency and use in e-CTD as agreed at the Washington DC Meeting, September 11-12, 2002)
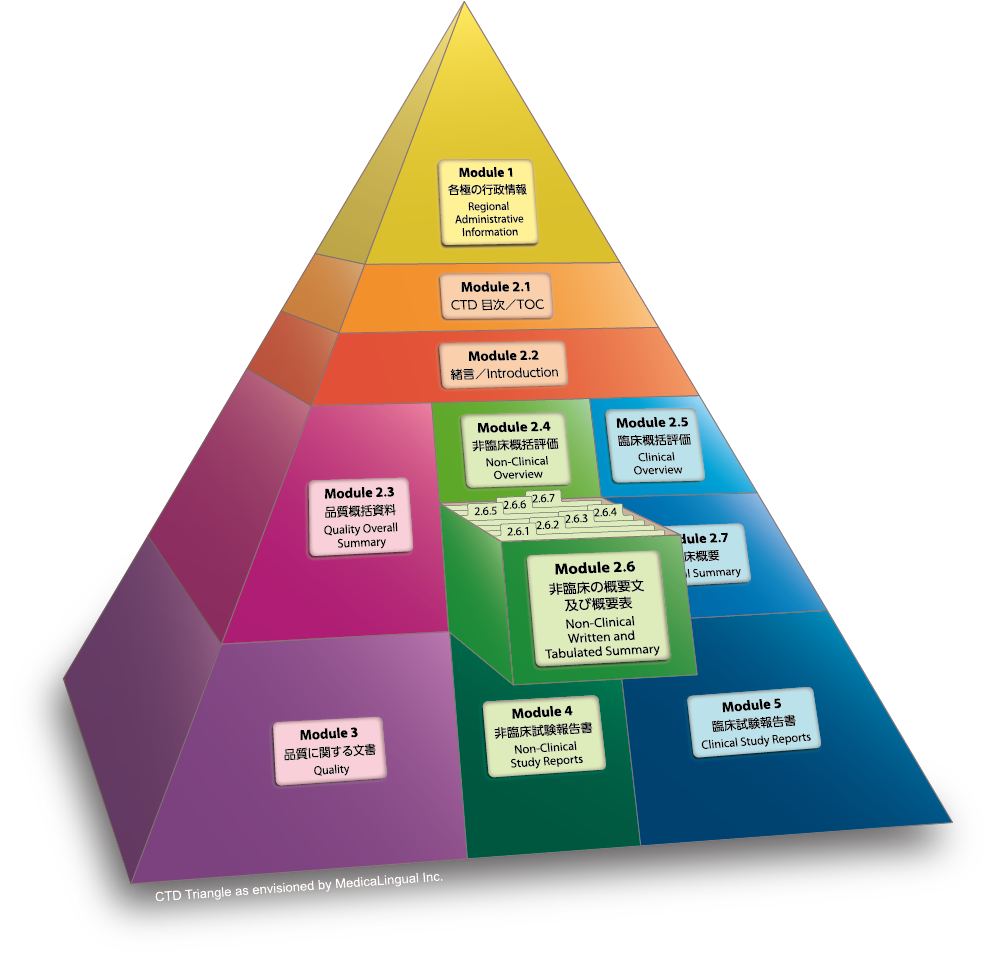
Module 2.6 非臨床試験の概要文及び概要表
2.6.4 薬物動態試験の概要文
薬物動態試験概要文の配列は以下に従うこと。
- まとめ
- 分析法
- 吸収
- 分布
- 代謝
- 排泄
- 薬物動態学的薬物相互作用
- その他の薬物動態試験
- 考察及び結論
- 図表(本文末尾又は本文中)
Module 2.6 NONCLINICAL WRITTEN AND TABULATED SUMMARIES
2.6.4 Pharmacokinetics Written Summary
The sequence of the Pharmacokinetics Written Summary should be as follows:
- Brief Summary
- Methods of Analysis
- Absorption
- Distribution
- Metabolism
- Excretion
- Pharmacokinetic Drug Interactions
- Other Pharmacokinetic Studies
- Discussion and Conclusions
- Tables and Figures (either here or included in text)
2.6.4.1 まとめ
薬物動態試験で得られた主要な所見を2~3頁に簡潔に要約すること。本項では、薬物動態学的評価に関する記述からはじめ、例えば検討した動物種及び系統が薬理試験及び毒性試験で使用されたものと同一かどうか、あるいは用いた投与形態が類似又は同一であったかどうかを明確にすること。
2.6.4.1 Brief Summary
The principal findings from the pharmacokinetics studies should be briefly summarized in approximately 2 to 3 pages. This section should begin with a description of the scope of the pharmacokinetic evaluation, emphasising, for example, whether the species and strains examined were those used in the pharmacology and toxicology evaluations, and whether the formulations used were similar or identical.
2.6.4.2 分析法
本項では、生体試料中の分析法に関して分析法の検出限界及び定量限界を含めて簡潔に要約すること。可能であれば、分析法のバリデーションデータや生体試料中の安定性についても考察すること。異なった分析法が結果の解釈に影響を及ぼす可能性については、以下の該当する項で考察すること。
2.6.4.2 Methods of Analysis
This section should contain a brief summary of the methods of analysis for biological samples, including the detection and quantification limits of an analytical procedure. If possible, validation data for the analytical method and stability of biological samples should be discussed in this section. The potential impact of different methods of analysis on the interpretation of the results should be discussed in the following relevant sections.
2.6.4.3 吸収
以下のデータを本項で要約すること。
- 吸収(吸収の程度と速度、In Vivo及びIn Situ試験)
- 薬物動態パラメータ、生物学的同等性及びバイオアベイラビリティ(血清、血漿及び全血)
2.6.4.3 Absorption
The following data should be summarised in this section:
- Absorption (extent and rate of absorption, in vivo and in situ studies)
- Kinetic parameters, bioequivalence and/or bioavailability (serum/plasma/blood PK studies)
2.6.4.4 分布
以下のデータを本項で要約すること。
- 組織分布試験
- たん白結合及び血球中への移行
- 胎盤通過試験
2.6.4.4 Distribution
The following data should be summarised in this section:
- Tissue distribution studies
- Protein binding and distribution in blood cells
- Placental transfer studies
2.6.4.5 代謝(動物種間の比較)
以下のデータを本項で要約すること。
- 生体試料中の代謝物の化学構造及び含有量
- 推定代謝経路
- 初回通過代謝(消化管及び肝初回通過効果)
- In Vitro代謝試験
- 酵素誘導及び阻害
2.6.4.5 Metabolism (interspecies comparison)
The following data should be summarised in this section:
- Chemical structures and quantities of metabolites in biological samples
- Possible metabolic pathways
- Pre-systemic metabolism (GI/hepatic first-pass effects)
- In vitro metabolism including P450 studies
- Enzyme induction and inhibition
2.6.4.6 排泄
以下のデータを本項で要約すること。
- 排泄の経路及び程度
- 乳汁排泄
2.6.4.6 Excretion
The following data should be summarised in this section:
- Routes and extent of excretion
- Excretion in milk
2.6.4.7 薬物動態学的薬物相互作用
非臨床の薬物動態学的薬物相互作用試験( In Vitro及びIn Vivo)が実施されている場合は、本項で簡潔に要約すること。
2.6.4.7 Pharmacokinetic Drug Interactions
If they have been performed, nonclinical pharmacokinetic drug-interaction studies (in vitro and/or in vivo) should be briefly summarised in this section.
2.6.4.8 その他の薬物動態試験
病態(腎障害等)モデルを用いた試験が実施されている場合は、本項で要約すること。
2.6.4.8 Other Pharmacokinetic Studies
If studies have been performed in nonclinical models of disease (e.g., renally impaired animals), they should be summarised in this section.
2.6.4.9 考察及び結論
本項では、薬物動態学的評価を考察し、また生じた問題の意義を論じること。
2.6.4.9 Discussion and Conclusions
This section provides an opportunity to discuss the pharmacokinetic evaluation and to consider the significance of any issues that arise.
2.6.4.10 図表
本文中の図表は、本文中の適切な場所又は本文末尾のいずれに入れても差し支えない。
2.6.4.10 Tables and Figures
Text tables and figures can be included at appropriate points throughout the summary within the text. Alternatively, there is the option of including tables and figures at the end of the summary.










