医薬審発第899号 CTD通知(別紙 3)
CTD-品質に関する文書の作成要領に関するガイドライン
(2002年9月11-12日ワシントン会議修正版)
ICH HARMONISED GUIDELINE
QUALITY – M4Q –
(Numbering and Section Headers have been edited for consistency and use in e-CTD as agreed at the Washington DC Meeting, September 11-12, 2002)
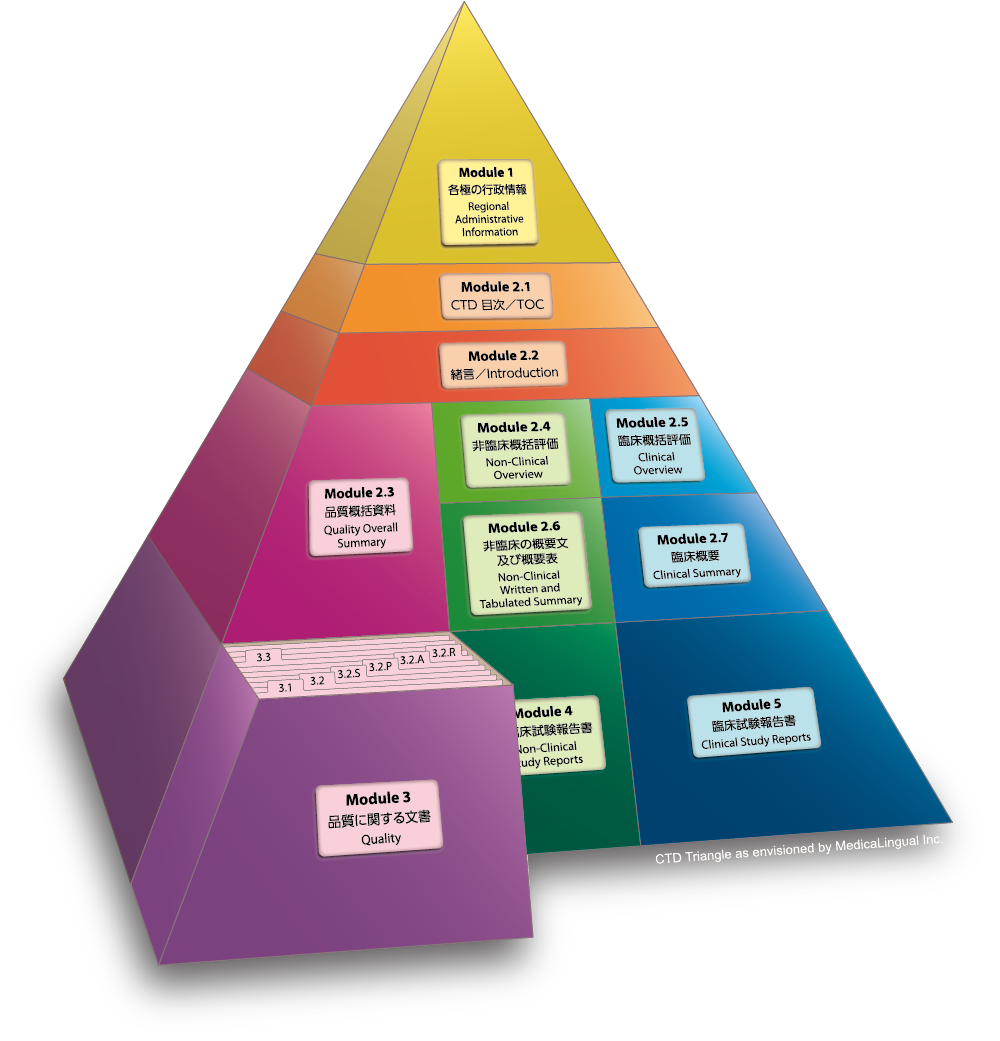
Module 3 品質に関する文書
3.2 データ
3.2.P 製剤
3.2.P.6 標準品又は標準物質
3.2.S.5 の項に記載していない標準品又は標準物質を製剤の試験に用いる場合には、それらに関する情報を記載する。
参照ICHガイドラインQ6A及びQ6B
Module 3 QUALITY
3.2 Body of Data
3.2.P Drug Product
3.2.P.6 Reference Standards or Materials
Information on the reference standards or reference materials used for testing of the drug product should be provided, if not previously provided in “3.2.S.5 Reference Standards or Materials”.
Reference ICH Guidelines: Q6A and Q6B










