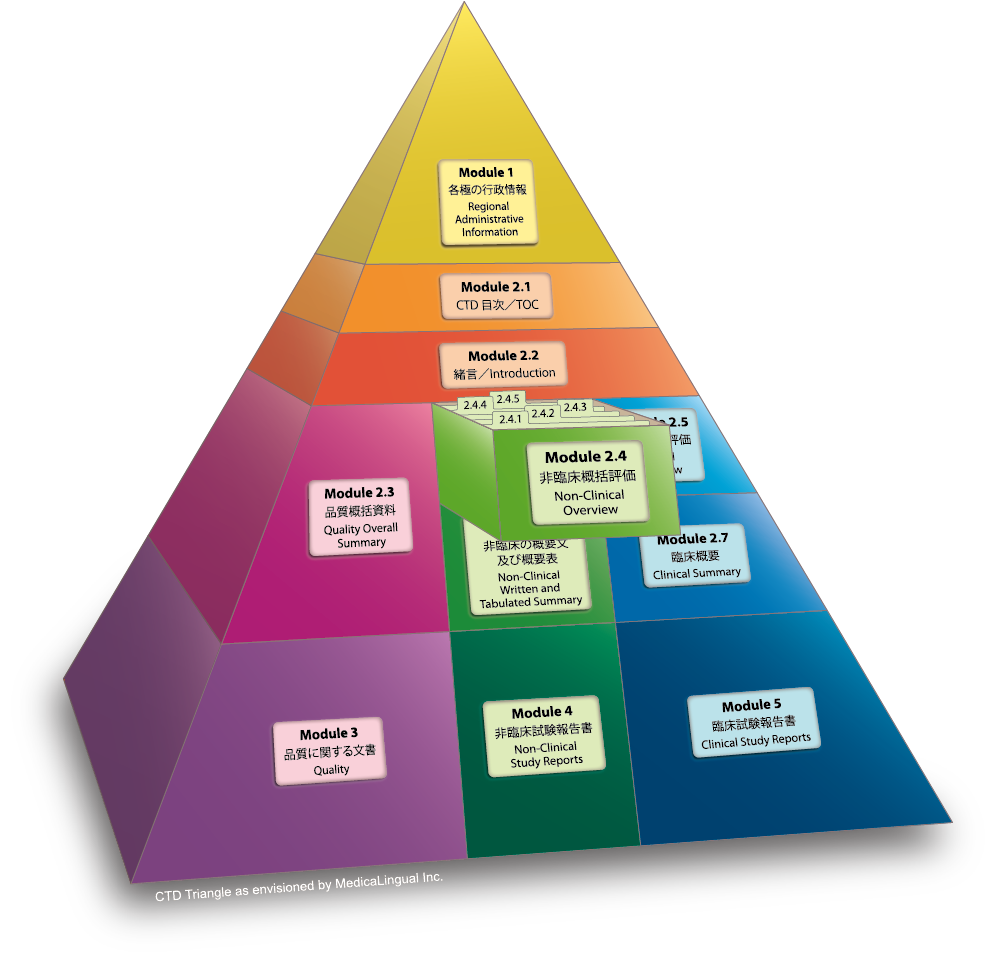
Module 2.4 非臨床に関する概括評価
2.4.1 非臨床試験計画概略
非臨床試験の概括評価では、医薬品の薬理評価、薬物動態評価及び毒性評価について包括的で客観的な評価結果を示すこと。試験の実施に関連するガイドラインがある場合には、ガイドラインを考慮するとともに、ガイドラインからの逸脱については、考察しその妥当性を示すこと。非臨床試験の計画についても、考察し妥当性を示すこと。提出された試験がGLPに適合していることについて示し、必要に応じて、非臨床試験で得られた所見と医薬品の品質、臨床試験の結果及び類薬で認められた作用との関連を示すこと。
Module 2.4 NONCLINICAL OVERVIEW
2.4.1 Overview of the Nonclinical Testing Strategy
The Nonclinical Overview should present an integrated and critical assessment of the pharmacologic, pharmacokinetic, and toxicologic evaluation of the pharmaceutical. Where relevant guidelines on the conduct of studies exist, these should be taken into consideration, and any deviation from these guidelines should be discussed and justified. The nonclinical testing strategy should be discussed and justified. There should be comment on the GLP status of the studies submitted. Any association between nonclinical findings and the quality characteristics of the human pharmaceutical, the results of clinical trials, or effects seen with related products should be indicated, as appropriate.
バイオテクノロジー応用医薬品を除き、原薬及び製剤中に含まれる不純物と分解物について評価し、推測される薬理及び毒性作用に関して判明している点についても示すこと。この際、原薬及び製剤について定められた不純物の上限が適切であることを示し、品質に関する資料との間で相互参照できるように記載すること。また、非臨床試験で用いた化合物と市販予定製品の間の光学活性、化学形態及び不純物プロフィールの相違について示すこと。バイオテクノロジー応用医薬品については非臨床試験で用いられた物質、臨床試験で用いられた物質及び市販予定製品である物質の同等性の評価結果を示すこと。新添加剤*を含む製剤の場合は、その安全性に関する情報を示すこと。
*使用前例のない,又は使用前例があっても投与経路が異なる若しくは前例を上回る量を使用する場合(邦訳時追記)
Except for biotechnology-derived products, an assessment of the impurities and degradants present in the drug substance and product should be included along with what is known of their potential pharmacologic and toxicologic effects. This assessment should form part of the justification for proposed impurity limits in the drug substance and product, and be appropriately cross-referenced to the quality documentation. The implications of any differences in the chirality, chemical form, and impurity profile between the compound used in the nonclinical studies and the product to be marketed should be discussed. For biotechnology-derived products, comparability of material used in nonclinical studies, clinical studies, and proposed for marketing should be assessed. If a drug product includes a novel excipient, an assessment of the information regarding its safety should be provided.
関連する科学論文及び類薬の特性を考慮すること。申請者が試験を実施する代わりとして、公表科学論文を引用する場合には、試験計画及び現行のガイドラインからの逸脱について考察し、妥当性を示すこと。また、これらの引用された試験で使用された原薬のバッチの品質に関する情報の入手可能性についても示すこと。
非臨床試験の概括評価において、概要表を引用する場合は表X.X, 試験/報告書番号とすること。
Relevant scientific literature and the properties of related products should be taken into account. If detailed references to published scientific literature are to be used in place of studies conducted by the applicant, this should be supported by an appropriate justification that reviews the design of the studies and any deviations from available guidelines. In addition, the availability of information on the quality of batches of drug substance used in these referenced studies should be discussed.
The Nonclinical Overview should contain appropriate reference citations to the Tabulated Summaries, in the following format: (Table X.X, Study/Report Number).










